cGMP-konformes Coriolis-Durchflussmessgerät für Single-Use-Anwendungen in der Biotechnologie
Single-Use-Technologien gewinnen in der Entwicklung und biotechnologischen Produktion neuer Wirkstoffe zunehmend an Bedeutung. Dies liegt an veränderten Prozessen und der fortschreitenden Personalisierung von Medikamenten und Therapien. Neue Lösungen in der Durchflussmesstechnik ermöglichen den Einsatz von wirtschaftlichen und sicheren Single-Use-Anlagen nicht nur im Batch-, sondern auch im kontinuierlichen Prozess. Zell- und genbasierte Therapien sind in der biopharmazeutischen Forschung als Schlüsseltechnologien etabliert und eröffnen neue therapeutische Ansätze.
Autor: Frank Jablonski, mylk+honey, für Endress+Hauser
Kontinuierlich und präzise: Neue Lösungen für die Durchflussmesstechnik in der biotechnologischen Produktion.

Zell- und genbasierte Therapien sind in der biopharmazeutischen Forschung längst als Schlüsseltechnologien angekommen. Sie öffnen Türen, um zukünftige Innovationen in der biomedizinischen Krankenversorgung zu erarbeiten. So ist bspw. die mRNA-Technologie als Durchbruch in der Impfstoffentwicklung in der Coronapandemie besonders sichtbar geworden. Die hier genutzte Boten-Ribonukleinsäure bildet gemeinsam mit weiteren neuen Wirkstoffklassen und Konzepten wie Antikörper- und Zelltherapien oder viralen Vektoren neue therapeutische Ansätze, die über die Immunisierung gegen Viruskrankheiten hinausgehen. Sie spielen darüber hinaus eine wachsende Rolle auch in der Behandlung von Tuberkulose, Malaria oder Krebs.
Dass die Bedeutung solch neuer Ansätze zunimmt, sieht man auch daran, dass immer mehr Wirkstoffe die klinischen Phasen erfolgreich durchlaufen und bei den Patienten ankommen: Etwa ein Viertel der Medikamente, die im laufenden Jahr in der Europäischen Union eingeführt werden sollen, könnte bspw. Menschen mit ganz unterschiedlichen Krebsarten zugutekommen.
Doch vor Markteinführung sind unzählige Testläufe und zahlreiche klinische Studien notwendig. In den Laboren müssen zahllose Varianten hergestellt und getestet werden, damit einige wenige Wirkstoffe den Weg bis zum Patienten schaffen. Die Komplexität nimmt zu und die Batch-Größen nehmen ab. Hinzu kommt, dass Therapien immer weiter individualisiert werden. Insgesamt führt dies in der Pharmaindustrie zu einem deutlichen Trend hin zu dynamischeren und hoch flexiblen Prozessen. Das gilt nicht nur für die Forschung: Es wird auch immer mehr zum Qualitätsmerkmal in der pharmazeutischen Produktion, agil auf dynamische Nachfragesituationen am Markt reagieren zu können.
Inhalt:
- Kontinuierlich und präzise: Neue Lösungen für die Durchflussmesstechnik in der biotechnologischen Produktion.
- Single-Use spart Reinigungs- und Energiekosten
- Coriolis: Schlüssel für kontinuierliche Produktion
- Lösungsfindung auf den zweiten Blick
- Messtechnologie und Materialauswahl führt zu Präzision
- Vorkalibrierte Einwegkomponente wird automatisch erkannt
- CITplus Wissen
Single-Use spart Reinigungs- und Energiekosten
Um diesen Herausforderungen zu begegnen, nutzen immer mehr Prozesse Single-Use-Systeme. Ihr Vorteil besteht vor allem darin, aufwändige Reinigungsprozesse wie bspw. die Verfahren Clean-in-Place (CIP) oder Steam-in-Place (SIP) zu minimieren. Dies spart Reinigungs- und Energiekosten und verringert chemische Abfälle der Reinigungslaugen. Vor allem jedoch vermeiden sie Kreuzkontaminationen. Daher sind sie schon lange integraler Bestandteil der biopharmazeutischen Produktion, besonders im Labor- und Pilotmaßstab, aber auch in der Produktion von Biopharmazeutika und Biosimilars. Einweg-Bioreaktoren und -Mischer mit Volumina bis zu 6.000 l sind keine Seltenheit.
Eine weitere Möglichkeit die Vorlaufzeiten zu minimieren und insgesamt agiler zu forschen und zu produzieren, ist die Prozessintensivierung. Kleinere und kompaktere Anlagen sind flexibler nutzbar und reduzieren Material- und Energieverbräuche. Der Weg von der klassischen Batch-Verfahrensweise zur kontinuierlichen Herstellung kann zudem in geringeren Betriebs- und Investitionskosten resultieren und eine höhere Betriebssicherheit zur Folge haben.
Coriolis: Schlüssel für kontinuierliche Produktion

Neue Reaktor-, Anlagen- und Prozesskonzepte benötigen jedoch auch eine entsprechende Verfahrenstechnik. Die Instrumentierung muss ein auf die Life-Sciences-Industrie und den neuen Konzepten zugeschnittenes Portfolio anbieten. Beispiel Durchflussmessung: Um eine kleine, agile, cGMP-gerechte Single-Use-Bioprozesstechnologie aufzubauen, sind hochgenaue Messgeräte unabdingbar. Mit dem Coriolis-Durchflussmessgerät Proline Promass U 500 hat Endress+Hauser ein Gerät entwickelt, dass sich nahtlos in die Automatisierungslandschaft einfügt. Auch Aspekte wie Reproduzierbarkeit, Konformität mit internationalen Regularien, Rückführbarkeit, Kalibrierung oder cGMP-Konformität werden erfüllt. Bei der Entwicklung mit OEM-Kunden hat sich das Team eng an den Anforderungskatalogen und Empfehlungen der Biotech-Plattform BioForum orientiert.
Lösungsfindung auf den zweiten Blick
Doch wie war eine solche Entwicklung möglich? Denn auf den ersten Blick bringen Verfahrensingenieure die beiden Aspekte Coriolis-Durchflussmessgerät und Single-Use nicht miteinander in Verbindung. Dafür war diese Durchflussmessmethode bislang deutlich zu teuer. Der Trick der Endress+Hauser Produkt- und Applikationsingenieure in der Neuentwicklung bestand darin, die Funktionseinheiten voneinander lösbar zu gestalten. So besteht Proline Promass U 500 aus einer Basiseinheit, die die Komponenten zur Spannungsversorgung, Erreger und Sensorik sowie die sonstige Elektronik enthält. Diese Basiseinheit gibt es in zwei funktionsgleichen Versionen: zum einen als Einbau-Ausführung, die OEM-Hersteller in ihre Plattformen integrieren können und zum anderen als Tabletop-Version in einem eigenen Gehäuse. Sie besitzt die entsprechenden Anschlüsse an die Laborumgebung vor Ort.
Diese Trennung der Funktionseinheiten führt dazu, dass das gesamte System als Single-Use-Durchflussmessung konzipiert werden konnte und dennoch sowohl für eine wirtschaftliche als auch eine präzise Durchflussmessung eingesetzt werden kann. Das Schwingungsrohr der Einwegkomponente besteht aus Edelstahl 316L (AISI) bzw. 1.4435 (EN), damit die Coriolis-Technologie ihre Stärken voll ausspielen kann: höchste Genauigkeit bei der gleichzeitigen Messung von Durchfluss, Temperatur und Dichte. Auf diese Weise setzt sich die Technologie auch deutlich von alternativen Verfahren wie beispielsweise gravimetrischen Messungen ab.
Messtechnologie und Materialauswahl führt zu Präzision
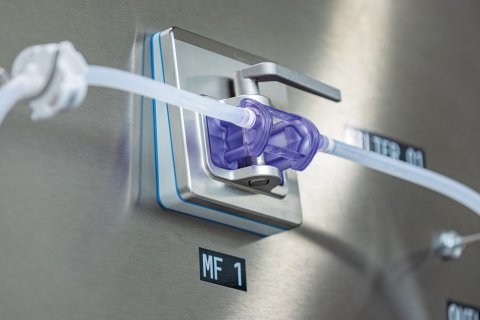
„Auch Vollkunststoff-Lösungen haben sich die Entwicklerinnen und Entwickler angeschaut, doch „das Schwingungsverhalten von Kunststoffen ist für die Coriolis-Technik nicht optimal“, erklärt Samuel Neeser, Produktmanager Coriolis bei Endress+Hauser Flow. „Unser Messrohr aus Edelstahl hingegen liefert präzise Ergebnisse, die sich mit Kunststoffrohren nicht erreichen lassen.“
Die Einwegkomponenten werden in vier unterschiedlichen Nennweiten angeboten und erreichen eine Messgenauigkeit von 0,5 % des Masseflusses. Betrachtet man den hohen Preis vieler Biopharmazeutika, bedeuten Messungenauigkeiten in der Tendenz schnell größere wirtschaftliche Nachteile. Somit amortisiert sich eine präzise Messtechnik, die alle prozesstechnischen Anforderungen erfüllt, schon nach kurzer Zeit.
Vorkalibrierte Einwegkomponente wird automatisch erkannt
Zu einem flexiblen und agilen Einsatz der Messeinrichtung gehört es auch, unnötige und fehleranfällige manuelle Tätigkeiten durch automatisierte zu ersetzen. Hier hat sich das Entwicklerteam einige besonders clevere Lösungen einfallen lassen. Zunächst einmal können die Einwegkomponenten von Proline Promass U 500 mit einer Hand in die Basiseinheit eingeschoben und verriegelt werden. Die Handgriffe lassen sich auch unter Reinraumbedingungen, das heißt mit entsprechender Schutzkleidung, einfach ausführen. Die dann normalerweise aufwändige und zeitraubende Kalibrierung vor Ort entfällt. Denn beim Einsetzen liest eine integrierte Kamera den bei der Werkskalibrierung aufgebrachten QR-Code und das Gerät startet eine automatische Verifizierung. Mithilfe der Heartbeat Technology von Endress+Hauser verifiziert die Basiseinheit die Gültigkeit der Werkskalibrierung. Das geführte Verfahren zur rückführbaren Verifizierung von Messgeräten nach ISO 9001 generiert zudem alle notwendigen Berichte.
Heartbeat Technology dokumentiert nicht nur die Funktionalität des Geräts, sondern liefert auch eine kontinuierliche Prozess- und Gerätediagnose im Sinne einer Zustandsüberwachung und sammelt Informationen zur Prozessoptimierung. Frühzeitige standardisierte Diagnosemeldungen mit Empfehlungen für eventuelle Behebungsmaßnahmen erhöhen die Betriebs- und Prozesssicherheit. Solche Optionen entfalten ihr Potenzial besonders in einer digitalen Produktionsumgebung. Das Gerät kommuniziert dazu via sicherem und raschem Datentransfer über 2-Draht Ethernet in Profinet- und Modbus-TCP-Netzwerken für die Anbindung an SPS-Systeme. Das Cloud-basierte Datenhandling erlaubt zudem prinzipiell den Zugriff unabhängig vom Standort.
Mit diesem Gesamtpaket ist ein Automatisierungsgrad in kontinuierlichen Single-Use-Prozessen angekommen, der in anderen Produktionen bereits Stand der Technik ist. Das ist besonders für Endanwender im Rahmen ihrer Qualitätssicherung nützlich, da der Dokumentations- und Zertifizierungsaufwand sowie die Kalibrierung der Einwegkomponente überschaubar bleiben. Auch bietet sich hier ein wesentlicher Baustein für die digitale Transformation der Biotechnologie. Insgesamt stößt das Coriolis-Durchflussgerät die Tür weit auf, die Forschung und Entwicklung neuer zell- und genbasierter Therapien zu beschleunigen und die Prozess-Intensivierung auch in die Produktion der noch jungen Wirkstoffklassen zu tragen.
CITplus Wissen
Herausforderungen bei der Herstellung von biotechnologischen Wirkstoffen und Hilfsmitteln
- Skalierbarkeit: Das Hochskalieren der Produktion von Labor- auf Industriemaßstab ist z. B. bei der Produktion monoklonaler Antikörper (mAbs) technisch anspruchsvoll.
- Stabilität: Beispielsweise mRNA ist sehr instabil und kann leicht abgebaut werden, was spezielle Formulierungen und Lagerungsbedingungen erfordert.
- Reinheit und Konsistenz: Sicherstellung der Reinheit und Konsistenz der Produkte durch präzise Prozesskontrolle und umfangreiche Reinigungsschritte.
- Kosten: Hohe Herstellungskosten aufgrund komplexer Produktionsverfahren und der Notwendigkeit strenger Qualitätskontrollen.
- Regulatorische Anforderungen: Strenge regulatorische Anforderungen und umfangreiche klinische Tests sind erforderlich, um Sicherheit und Wirksamkeit zu gewährleisten.
- Lagerung und Transport: Notwendigkeit extrem niedriger Temperaturen für die Lagerung und den Transport (z. B. 70 °C für einige mRNA-Impfstoffe).















