Keimdurchgang bei Reinraumbekleidung
Der Annex 1 des EU-GMP Leitfadens fordert u. a. eine Kontaminationskontrollstrategie. Diese soll sicherstellen, dass die gesamte Prozesskette auf mögliche Kontaminationsquellen überprüft wird und Maßnahmen ergriffen werden, um mikrobiologische und partikuläre Kontaminationen weitgehend auszuschließen. Die Wahl des richtigen Bekleidungssystems als einzige Barriere zwischen Personal und Umgebung/Produkt ist daher von größter Wichtigkeit. Doch wie wird der Keimdurchgang der eingesetzten Reinraumtextilien überprüft?
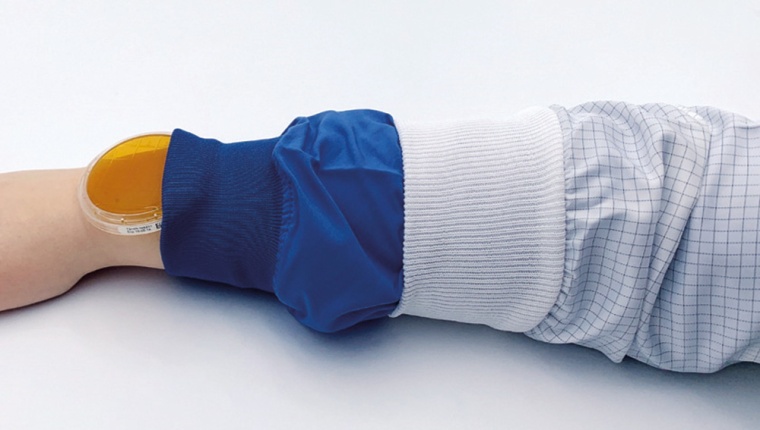
Der Keimdurchgang ist ein wichtiger Parameter zur Beurteilung von Reinraumbekleidung in den Life-Science-Anwendungen. Konkret stellt sich die Frage: Wie viele Keime der menschlichen Hautflora können durch die Bekleidung nach außen dringen? ( siehe Abb. oben)
Für die Untersuchung des Keimdurchgangs unter realitätsnahen Belastungen wurde eine neue Prüfmethode entwickelt. Die ersten Untersuchungsergebnisse zeigen, dass Mehrweg-Reinraumbekleidung bei entsprechender Auswahl des Reinraumbekleidungssystems sehr geringe Keimdurchgangswerte aufweist.
Bestehende Prüfmethoden für die Bestimmung des Keimdurchgangs
Wie wird das Barriereverhalten der eingesetzten Reinraumbekleidung gegenüber Bakterien überprüft? Hierbei sind mehrere teils genormte Verfahren in Betracht zu ziehen. In der Tabelle sind die Prüfverfahren vergleichend gegenübergestellt.

Prüfung der bakteriellen Filterleistung
Bei der Bestimmung der bakteriellen Filterleistung gemäß den Normen DIN EN 14683[1] und ASTM F2101-22[2], welche für die Prüfung medizinischer Gesichtsmasken vorgesehen sind, werden Aerosole mit Staphylococcus aureus-Bakterien in einem Kaskadenaufprallgerät aktiv durch die Messproben gesaugt. Das von der Firma Berner International für die Prüfung von Schutzkleidungsmaterialien modifizierte und vereinfachte Verfahren bedient sich des gleichen Testprinzips[3].
Hier werden jedoch Bakteriensporen eingesetzt, welche nicht Teil einer physiologischen Hautflora des Menschen sind. Für eine möglichst realitätsnahe Untersuchung des Keimdurchgangs bei Reinraumtextilien unter Berücksichtigung der Tragesituation scheinen Verfahren, welche Bakterien in Aerosolen einsetzen, weniger geeignet. Des Weiteren bildet ein aktives Durchsaugen die Situation beim Tragen von Reinraumbekleidung nur unzureichend ab: eine mechanische Belastung unter Bewegung scheint in diesem Fall realitätsnäher.
Prüfung des Keimdurchtritts im feuchten Zustand
Das genormte Verfahren nach DIN EN ISO 22610[4] für die Untersuchung der Widerstandsfähigkeit gegen Keimdurchtritt im feuchten Zustand wird zur Beurteilung des Keimdurchgangs bei OP-Textilien und Infektionsschutzkleidung gefordert. Bei diesem Verfahren ist die Materialprobe einer punktuellen mechanischen Belastung von 3 N ausgesetzt. Das sogenannte „Wet-Penetration“-Verfahren kann als sehr zeitintensiv und aufwändig eingestuft werden, da die als Keimempfänger eingesetzten Agarplatten nicht kommerziell zu beziehen sind und eine Standardisierung im Labor innerhalb vorgegebener enger Grenzen schwierig ist. Außerdem werden für jede Messprobe mit demselben Keimträger fünf Läufe von jeweils 15 Minuten sowie ein sechster Lauf zur Bestimmung der Keimzahl auf der Probenrückseite durchgeführt. Vermutlich basiert aufgrund dieser aufwändigen Vorgehensweise bei diesem Normverfahren eine Beurteilung der Barrierewirkung auf lediglich n=5 Messproben.
Neue Prüfmethode zur Bestimmung des Keimdurchgangs im feuchten Zustand
Diese bisher eingesetzten Prüfverfahren entsprechen nicht dem angestrebten Einsatz von möglichst realitätsnahen Prüfbedingungen für Reinraumbekleidung. Daher wurde in einem gemeinsamen Projekt von der Firma Dastex und den Deutschen Instituten für Textil- und Faserforschung Denkendorf (DITF) eine neue Prüfmethode entwickelt.
Basierend auf dem Testprinzip der DIN EN ISO 22610 sollte eine neue Prüfmethode zur Bestimmung des Keimdurchgangs (Bakterien) bei Reinraumtextilien unter realitätsnahen Bedingungen und mit hoher Flexibilität entwickelt werden. Die Anforderungen wurden folgendermaßen definiert:
- Mechanische Belastung unter Bewegung
- Flexible Einstellung der mechanischen Belastung
- Flexible Einstellung der Belastungsdauer
- Option der Simulation des Tragens von Zwischenbekleidung
- Option der Vorbenetzung mit (alkoholischen) Desinfektionsmitteln auf der Textilaußenseite
- Option der Simulation des Schwitzvorgangs auf der Textilinnenseite
- Zeitersparnis durch parallele Prüfung mehrerer Messproben eines Materials

ReBa2-Prüfmethode zur Bestimmung des Keimdurchgangs
Die neu entwickelte ReBa2 (Realitätsnahe Bakterienbarriere)-Prüfmethode wird den genannten Anforderungen gerecht.
Beschreibung der Methode
Das ReBa2-Prüfgerät (Abb. oben) verfügt über sechs identische Prüfstellen, wodurch es möglich ist, mehrere Messproben zeitgleich zu prüfen. Diese sind, wie in der folgeden Abbildung schematisch dargestellt, folgendermaßen von unten nach oben aufgebaut: Als Keimempfänger wird eine kommerziell erhältliche Abklatschplatte mit Universalmedium (nachfolgend Agar-Kontaktplatte genannt) eingesetzt, bei welcher die Agar-Oberfläche über den Schalenrand hinausragt. Diese dient außerdem als moderate Feuchtigkeitsquelle für das Gesamtsystem. Auf die Agar-Kontaktplatte werden zwei Lagen eines sterilen Baumwollgewebes aufgelegt. Dieses Baumwollgewebe dient als weiterer Keimempfänger und wird aus versuchstechnischen Gründen benötigt. Dadurch kann eine realitätsnahe Keimbelastung von über 105 Koloniebildenden Einheiten (KBE) pro Prüfung eingesetzt werden und, trotz hoher Keimbelastung, ist eine quantitative Bestimmung der durch die Messprobe migrierenden Keime möglich. Auf das Baumwollgewebe wird die Messprobe mit der Außenseite nach unten aufgelegt.

Bei einer Prüfung mit zusätzlichem Zwischenbekleidungstextil wird diese Probe auf die Messprobe des Reinraumtextils mit der Außenseite nach unten zeigend aufgelegt. Darauf wird der Keimträger positioniert. Als Keimträger werden Staphylococcus epidermidis-Bakterien auf einer Keimträgerfolie innerhalb einer markierten Fläche aufgebracht und unter der sterilen Werkbank angetrocknet. Die Abdeckung des Probenaufbaus zur Vermeidung von Feuchtigkeitsverlust und Kontaminationen erfolgt mittels einer dünnen Abdeckfolie. Abschließend wird der Probenaufbau fixiert. Danach wird pro Prüfstelle eine Edelstahlwalze als Gewicht in einer Halterung aufgelegt.
Während der Versuchsdurchführung gelangen die durch das Reinraumtextil migrierten Bakterien in die Keimempfänger. Die Keime verbleiben im Baumwollgewebe oder erreichen die darunterliegende Agar-Kontaktplatte. Die Anzahl der Koloniebildenden Einheiten (KBE) auf der Agar-Kontaktplatte wird nach der Bebrütung ermittelt. Die Bakterien im Baumwollgewebe werden durch Ausschütteln in Eluierungspuffer und einer kurzen Ultraschallbehandlung abgelöst. Die Keimzahl in der Bakteriensuspension wird mittels klassischer mikrobiologischer Verdünnungs- und Kulturmethoden bestimmt. Die Gesamtzahl der durch die Messprobe migrierten Keime wird aus der Anzahl der Keime aus dem Baumwollgewebe und der Anzahl der Keime auf der Kontaktplatte berechnet.
Zur Ermittlung des 100 %-Referenzwertes für den prozentualen Keimdurchgang erfolgt an einer der sechs Prüfstellen der Aufbau gleichermaßen, jedoch ohne Messprobe.
Als Kennwert für die Barrierewirkung gegenüber Bakterien wird bei der ReBa2-Prüfmethode der Keimdurchgang in Prozent angegeben. Eine Angabe des Rückhaltevermögens gegenüber Bakterien ist ebenfalls möglich, indem der Keimdurchgangswert von 100 subtrahiert wird.
Wahl der mechanischen Belastung und Belastungsdauer
Die geforderte realitätsnahe mechanische Belastung unter Bewegung wird durch die Gewichtskraft von frei beweglichen Edelstahlwalzen in Kombination mit einer langsamen, kontinuierlichen Hin- und Herbewegung der Prüfstellen unter den Walzen erreicht. Es besteht die Möglichkeit, verschiedene Edelstahlwalzen zu verwenden und somit unterschiedliche Belastungen nachzustellen. Der resultierende Druck auf die Kontaktfläche beträgt bei der vorzugsweise verwendeten Edelstahlwalze 1,7 N/cm2 (experimentell ermittelt) und liegt damit geringfügig über dem Druck von 1,4 N/cm2, welcher in der Literatur für ein starkes Aufstützen auf den Unterarm genannt wird[5]. Die Laufzeit des ReBa2-Prüfgeräts kann flexibel gewählt werden. Als realitätsnahe Belastungszeiten für Reinraumtextilien wurden 30 Minuten bis maximal zwei Stunden angenommen.
Auswahl des Prüfkeims
Um eine realitätsnahe bakterielle Belastung nachzustellen, wurde der Bakterien-Teststamm Staphylococcus epidermidis ausgewählt. Diese kugelförmigen, etwa 1 µm großen Bakterien zählen zu den häufigsten auf der Haut vertretenen Mikroorganismen einer Normalflora bei gesunden Menschen[6]. Die Anzahl von Keimen auf dem menschlichen Körper ist in den verschiedenen Hautregionen unterschiedlich groß. Generell ist die Keimzahl in feuchten Bereichen viel höher als in trockenen Hautregionen. Die bakterielle Keimbelastung (Inokulum) in der ReBa2-Prüfmethode beträgt 0,5–2 x 105 KBE/Keimträger. Bezogen auf die gewählte Kontaktfläche ist von einer bakteriellen Belastung auszugehen, welche die Hautbesiedlung von trockenen Hautregionen wie den Unterarmen bis hin zu feuchteren Bereichen abbilden kann.
Ergänzende Versuchseinstellungen
Bei einer Prüfung mit zusätzlichem Zwischenbekleidungsmaterial wird diese Probe im Probenaufbau auf die Messprobe des Reinraumtextils mit der Außenseite nach unten zeigend aufgelegt und befindet sich somit zwischen Reinraumtextil und Keimträger.
Soll eine mögliche Befeuchtung der Reinraumbekleidung nachgestellt werden, die insbesondere im Bereich der Vorderseite und der Ärmel durch Prozessflüssigkeiten oder Desinfektionsmittel auftreten kann, ist eine Vorbenetzung der Außenseite der Messprobe möglich.
Bei einer gewünschten zusätzlichen Simulation des Schwitzvorgangs kann die Innenseite der Reinraumtextilprobe oder der Zwischenbekleidungstextilprobe mit einer Schweißsimulanzlösung vorbenetzt werden.
Messunsicherheit der ReBa2-Prüfmethode
Die Messunsicherheit der ReBa2-Prüfmethode wurde bei vier Mehrweg-Reinraumtextilien mit einem Stichprobenumfang von jeweils n=30 ermittelt. Die Streuungen zeigten sich materialspezifisch und können daher nicht auf die gesamte Produktgruppe „Reinraumtextilien“ übertragen werden. Insgesamt können die ermittelten Messunsicherheiten als vergleichbar zu ähnlichen biologischen Verfahren bewertet werden.
Erste Studie mit Mehrweg- und Einweg-Reinraumtextilien
In einer umfassenden Versuchsreihe mit der neuen ReBa2-Prüfmethode wurde der Keimdurchgang von drei Mehrweg-Reinraumtextilien – jeweils mit und ohne Zwischenbekleidungstextil – sowie zwei Einweg-Overallmaterialien untersucht. Es handelt sich um Materialien, die in den Life-Science-Anwendungen in diesen Kombinationen zum Einsatz kommen.
Als Standard-Reinraumgewebe wurde das Material ION-Nostat VI.2 als Referenz mit in die Untersuchung einbezogen. Im Hinblick auf die Aufgabenstellung, Bakterien möglichst gut zurückzuhalten, waren zwei der drei Materialien für Mehrweg-Reinraumbekleidung mit einer wasserabweisenden Ausrüstung versehen (ION-Nostat VI.2 WA und Dastat-P). Als Zwischenbekleidungsmaterialien wurden Light Tech II (ZB 1) und Light Tech II AM (ZB 2) getestet.
Die Mehrweg-Materialien wurden im Neuzustand und im gealterten Zustand – erreicht durch 60 Dekontaminationswäschen/Dampfsterilisationen (60 DS) bei den Reinraumbekleidungstextilien bzw. durch 10 Dekontaminationswäschen (10 D) bei den Zwischenbekleidungsmaterialien – untersucht. 60 Aufbereitungszyklen entsprechen der durchschnittlichen empfohlenen Lebensdauer von Mehrweg-Reinraumbekleidung, wenn diese dampfsterilisiert wird.
Als Versuchsbedingungen wurden eine mechanische Belastung von 1,7 N/cm2 für eine Zeitdauer von zwei Stunden ohne eine zusätzliche Simulation des Schwitzvorgangs oder eine Vorbenetzung der Textilaußenseite gewählt. Die Anzahl der Messproben wurde mit jeweils n=10 festgelegt.
Wie im Ergebnisdiagramm dargestellt, zeigte das Material ION-Nostat VI.2 für Mehrweg-Reinraumbekleidung einen vergleichbaren Keimdurchgang wie die beiden getesteten Einweg-Overallmaterialien (Einweg A und Einweg B).
Bei den Materialien ION-Nostat VI.2 WA und Dastat-P mit wasserabweisender Ausrüstung konnte kein nennenswerter Keimdurchgang (< 1 %) ermittelt werden.

Der Einsatz von Reinraumzwischenbekleidungsmaterial reduzierte den Keimdurchgang beim Reinraumgewebe ION-Nostat VI.2 um ca. 50 %. Bei den Materialien mit wasserabweisender Ausrüstung war in Verbindung mit dem Zwischenbekleidungsmaterial der Keimdurchgang unterhalb der Nachweisgrenze.
Bei keinem der getesteten Mehrweg-Reinraumtextilien war ein signifikanter Unterschied der Keimdurchgangswerte vor und nach der Alterungsbehandlung zu ermitteln. Bei ION-Nostat VI.2 und ION-Nostat VI.2 WA wurde tendenziell eine Verringerung des Keimdurchgangs, bei Dastat-P dagegen eine Erhöhung des Keimdurchgangs festgestellt.
Auch bei den gealterten Mehrwegmaterialien in Kombination mit den ebenfalls gealterten Zwischenbekleidungsmaterialien wurden deutlich geringere Keimdurchgangswerte festgestellt – vergleichbar mit den Versuchsergebnissen vor der Alterungsbehandlung. Bei ION-Nostat VI.2 betrug die Reduktion bei Einsatz von Zwischenbekleidungsmaterial auch im gealterten Zustand mehr als 50 %.
Die Streuung der Keimdurchgangswerte liegt bei den Einwegmaterialien höher als bei den Mehrwegtextilien. Nach der Alterung wurde bei den Mehrwegtextilien tendenziell ebenfalls eine größere Streuung der Keimdurchgangswerte festgestellt.
Diskussion der Ergebnisse
Die Untersuchungsergebnisse zeigen, dass das besonders atmungsaktive Gewebe ION-Nostat VI.2 gegenüber Bakterien eine ebenso gute Barriere bietet wie die als Chemikalienschutzkleidung Typ 5/6 gekennzeichneten getesteten Einwegmaterialien. Wird das Gewebe ION-Nostat VI.2 zusätzlich wasserabweisend ausgerüstet (WA), hält es Bakterien bei feuchten Umgebungsbedingungen weitgehend zurück, sogar etwas besser als das ebenfalls wasserabweisend ausgerüstete Gewebe Dastat-P mit deutlich geringerer Luftdurchlässigkeit.
Tendenziell ist bei den gealterten ION-Nostat VI.2-Geweben eine Reduktion der Keimdurchgangswerte zu sehen. Bei Dastat-P sind die Keimdurchgangswerte nach der Alterungsbehandlung erhöht, jedoch ohne statistische Signifikanz. Eine mögliche Erklärung dafür könnte zum einen in einem teilweisen Auswaschen der Ausrüstung, zum anderen auch in der Reduzierung der durch Kalandrierung erzielten Verdichtung des Gewebes liegen. Die verdichtende Wirkung einer Kalandrierung kann erfahrungsgemäß bereits nach wenigen Wäschen reduziert sein.
Der Einsatz einer Reinraumzwischenbekleidung reduziert den Keimdurchgang auch bei dem besonders atmungsaktiven Gewebe ION-Nostat VI.2 ohne wasserabweisende Ausrüstung um ca. 50 %, bei den Geweben mit wasserabweisender Ausrüstung bis zur Nachweisgrenze. Eine Migration der Keime durch mehrere Textillagen scheint deutlich erschwert, wobei zwischen den beiden getesteten Zwischenbekleidungsmaterialien kein signifikanter Unterschied aufgezeigt werden konnte.
Der relativ hohe Keimdurchgang bei der als Chemikalienschutzkleidung mit zusätzlicher Schutzfunktion gegenüber biologischen Kontaminationen (Typ 5B und 6B) gekennzeichneten Einweg-Reinraumbekleidung (Einweg A) deckt sich mit dem technischen Datenblatt des Herstellers. Laut den dort genannten Werten wurde das Einwegprodukt bei der ähnlichen Prüfung nach DIN EN ISO 22610 (Keimdurchtritt bei Feuchte) in der niedrigsten Klasse (≤ 15 min) eingestuft. Neben der optisch erkennbaren Materialungleichmäßigkeit des Vliesstoffmaterials, die auch in den großen Streuungen der Werte erkennbar ist, spielt vermutlich auch die geringe Dicke (175 µm) des leichten Materials (ca. 45 g/m²) eine Rolle bei der Durchdringung der Bakterien bei feuchten Umgebungsbedingungen unter mechanischer Belastung. Der Einfluss der Materialdicke war bei den Versuchen mit Zwischenbekleidungsmaterial deutlich erkennbar.
Fazit
Die Ergebnisse der Untersuchungen zeigen, dass Mehrweg-Reinraumbekleidung bei entsprechender Materialauswahl und dem Einsatz einer Zwischenbekleidung Keime sehr gut über die gesamte empfohlene Lebensdauer zurückhalten kann.
Für bestmöglichen Schutz ist auch die Kombination verschiedener Gewebe in einem Kleidungsstück denkbar, z.B. könnte in besonders kritischen Bereichen wie den Ärmeln ein Material mit geringstem Keimdurchgang verarbeitet werden.
Die neue ReBa2-Prüfmethode bietet durch ihre Realitätsnähe zahlreiche Vorteile gegenüber den bisherigen Verfahren. Mit dem konzipierten Aufbau sind zahlreiche Prüfszenarien möglich. Neben einzelnen Textilien können Textilkombinationen, mit Desinfektionsmitteln oder Schweißsimulanz vorbenetzte Textilien usw. mit aussagekräftiger Messprobenanzahl untersucht werden. Die neue ReBa2-Prüfmethode steht an den DITF Denkendorf ab sofort zur Verfügung.
Hinweis: Alle diskutierten technischen Daten zu den Mehrweg-Materialien sind über die unten genannte Homepage einsehbar.
Literatur:
[1] DIN EN 14683:2019-10 Medizinische Gesichtsmasken – Anforderungen und Prüfverfahren
[2] ASTM F2101-22 Standard Test Method for Evaluating the Bacterial Filtration Efficiency (BFE) of Medical Face Mask Materials, Using a Biological Aerosol of Staphylococcus aureus
[3] Berner International GmbH,
https://www.berner-safety.de/reinraum_schutzkleidung_eine_barriere_fuer_bakterien_de_1474.html, abgerufen am 06.03.2023 um 15:08 Uhr siehe auch Jedamski, L.; Dieckhoff, M.; Klein, M. (2016): Bakterienrückhalt Schutzkleidungsmaterialien für die Zytostatika-Zubereitung im Test, Onkologische Pharmazie; Nr. 4/2016, S. 40 - 44
[4] DIN EN ISO 22610: 2006-10 Operationsabdecktücher, -mäntel und Rein-Luft-Kleidung zur Verwendung als Medizinprodukte für Patienten, Klinikpersonal und Geräte-Prüfverfahren für die Widerstandsfähigkeit gegen Keimdurchtritt im feuchten Zustand
[5] Rabe, M. (1999): Analyse und Optimierung der Barrierewirkung textiler Fügeverbindungen gegenüber kontaminierten Körperflüssigkeiten am Beispiel von OP-Systemen, Dissertation, Shaker Verlag, Aachen, S. 57
[6] Marenbach, D. (2007): Untersuchung zur Verteilung von Bakterien in der menschlichen Haut (Dissertation), S. 29
Autoren
Alina Kopp, Carsten Moschner, Sarah Gaza, Forschung & Entwicklung, Geschäftsleitung, Qualitätsmanagement
Dastex Reinraumzubehör GmbH & Co. KG, Muggensturm
Evi Held-Föhn, Gabriele Schmeer-Lioe, Laborleitung Prüflabor Biologie, Laborleitung Prüflabor Reinraumtextilien und Elektrostatisches Verhalten Deutsche Institute für Textil- und Faserforschung Denkendorf
Mitautoren
Götz T. Gresser, Institutsleitung und Vorstand, Deutsche Institute für Textil- und Faserforschung Denkendorf
Carsten Linti, Leitung Technologiezentrum Biomedizintechnik, Deutsche Institute für Textil- und Faserforschung Denkendorf
Thomas Stegmaier, Leitung KPZ Textilchemie, Umwelt & Energie, Deutsche Institute für Textil- und Faserforschung Denkendorf














